主な利点
-
候補者を見逃さない
指向性進化と合理的設計を組み合わせる -
信頼できるデータ
動物実験における統合されたデータ -
独占的かつ機密
今後のプロジェクトでは、検証済みの変異配列は使用されず、削除されます
サービスの詳細
PackGene の π-lcosa AAV キャプシドエンジニアリングサービスはどのようなことができるのでしょうか?
- 標的細胞への遺伝子導入の特異性と効率を高めます。
- オフターゲット効果や不要な免疫応答のリスクを最小限に抑えます。
- がんや遺伝性疾患に対する治療法を、特定の疾患や症状を治療する上でより精密かつ効果的なものとして設計します。
当社の標準的なキャプシドエンジニアリングサービスには、キャプシドライブラリーの設計・構築、2 ラウンドのスクリーニング、そしてモデル動物におけるトップバリアントの性能の最終検証が含まれます。ご自身のスクリーニング基準、動物試験、およびカスタマイズされたご要望につきましては、技術サポートとご相談ください。
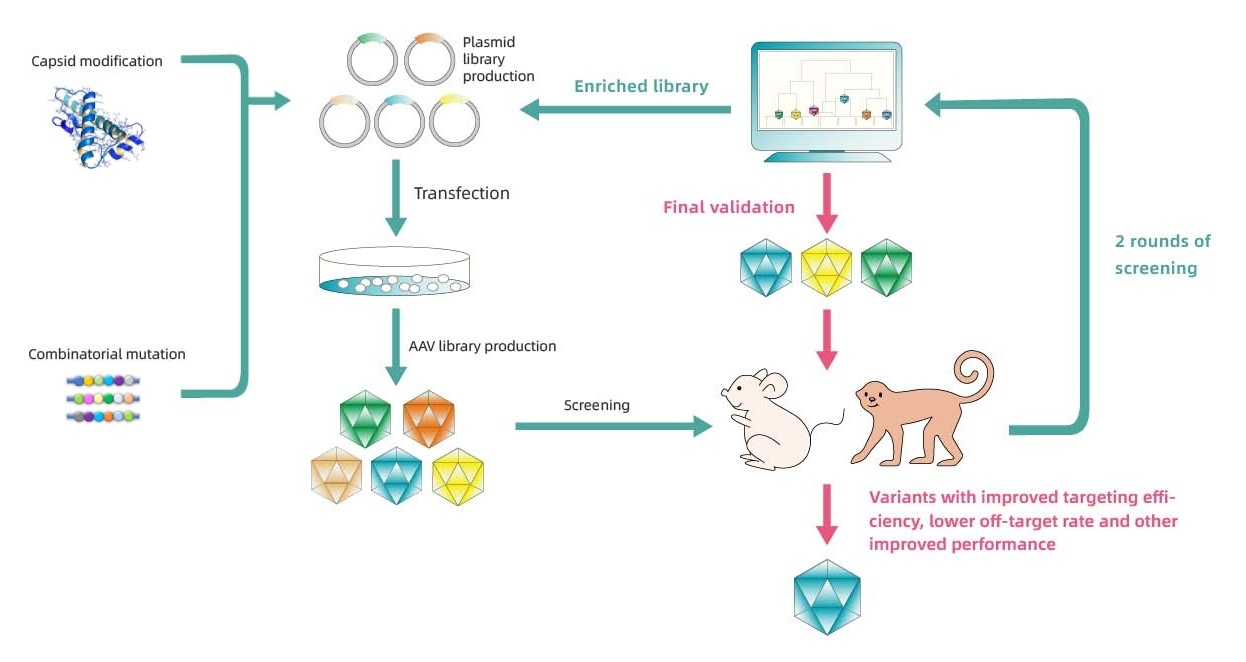
キャプシドエンジニアリングの詳細なワークフロー
PackGene は、AAV キャプシドエンジニアリングプラットフォームである π-lcosa システムを開発しており、カスタマイズされたご要望に応じて、臓器感染性が高められた、オフターゲット性が低下した、あるいはその他の特徴を持つ AAV キャプシドバリアント配列を操作・スクリーニングすることができます。このプロセスには、CCT(臨床センター試験)での潜在的な使用のためのトップバリアントを特定するために、AAV キャプシドライブラリーの構築と動物でのスクリーニングを 3 段階に分けて行います。フェーズ I には、キャプシドライブラリーの初期構築、AAV パッケージング、動物への投与、および動物試験が含まれ、その後 NGS 解析と、必要であればラウンド 2 のライブラリー設計が行われます。フェーズ II はフェーズ I のスクリーニング結果に基づいて改変されたライブラリーから始まり、トップバリアントを特定するために同様のプロセスに従います。フェーズ III では、トップバリアントプラスミドが構築され、AAV パッケージングが行われ、より大規模で動物への投与と試験が実施され、要望に応じて追加料金と時間を要する組織学的検査が可能です。このプロセスは、CCT 開発の必要性に応じて、最も効率的で特異的な AAV キャプシドを特定することを目的としています。 [π-lcosa テクノロジープラットフォームの詳細はこちらをクリック]
パフォーマンス
-
優れた入力ライブラリー品質
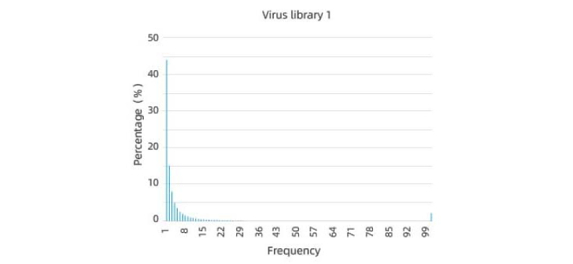
優れたスクリーニング前のライブラリー多様性と均一性
高いカバレッジのライブラリーには多くの異なるキャプシドバリアントが含まれており、望ましい特性を持つバリアントを見つける可能性が高まります。カバレッジの低いライブラリーでは重要なキャプシドバリアントが欠ける可能性があり、キャプシドエンジニアリングの可能性が制限されます。したがって、ライブラリーが多様で多数の異なるバリアントを含んでいることを確認することが重要です。
均一性も重要です。なぜなら、それぞれのキャプシドバリアントがライブラリー内で均等に表れることを保証するからです。不均一な表現はスクリーニングプロセスを歪め、望ましくないサブポピュレーションバリアントの選択につながる可能性があります。したがって、ライブラリーが均一に分布し、それぞれのバリアントが同様の量で表れていることを確認することが重要です。
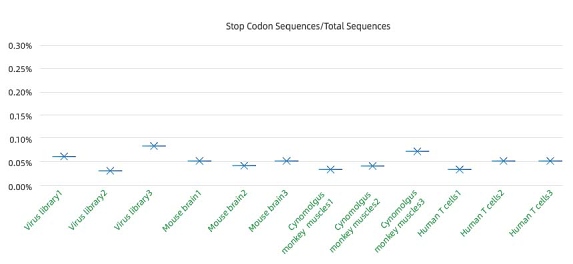
極めて低い誤パッケージング率: <0.1%
早期終結型キャプシド遺伝子を持つウイルスの割合は、誤パッケージング率の重要な指標です。高い誤パッケージング率は、キャプシド血清型とそれが含む実際のゲノムとの不一致につながり、スクリーニング結果に誤りを生じさせます。
AAV キャプシドエンジニアリングでは、AAV キャプシドを改変して効率性や特異性を向上させることが目標です。これを実現する一つの方法は、AAV バリアントのライブラリーを作製し、望ましい特性を持つバリアントをスクリーニングすることです。しかし、このライブラリーから生産される AAV ベクターの誤パッケージング率が高い場合、スクリーニング結果は不正確で信頼性がない可能性があります。
高い誤パッケージング率は、不正確な遺伝物質を含む AAV ベクターの生産につながる可能性があります。これらのベクターはその後、意図しない細胞や組織に形質導入する可能性があり、オフターゲット効果や不要な免疫応答を引き起こす可能性があります。これにより、がんや遺伝性疾患の治療法の安全性に悪影響を及ぼす可能性があります。
したがって、AAV キャプシドエンジニアリングにおける誤パッケージングを最小限に抑えることは重要です。これは、ベクター生産プロセス、例えば使用するプラスミドの品質を高めることや、意図されたキャプシドの表現が均等になるようにすること、さらに AAV ベクターの誤パッケージングについて慎重にスクリーニングすることなどによって達成できます。
誤パッケージング率を測定するために、我々は全集団における早期終結型キャプシドタンパク質を持つ AAV 集団の割合を測定します。結果は、我々が極めて低い誤パッケージング率を有していることを示しており、パッケージングされた AAV キャプシド遺伝子とキャプシドタンパク質の一致を保証し、それによって信頼性の高いスクリーニング結果につながります。
-
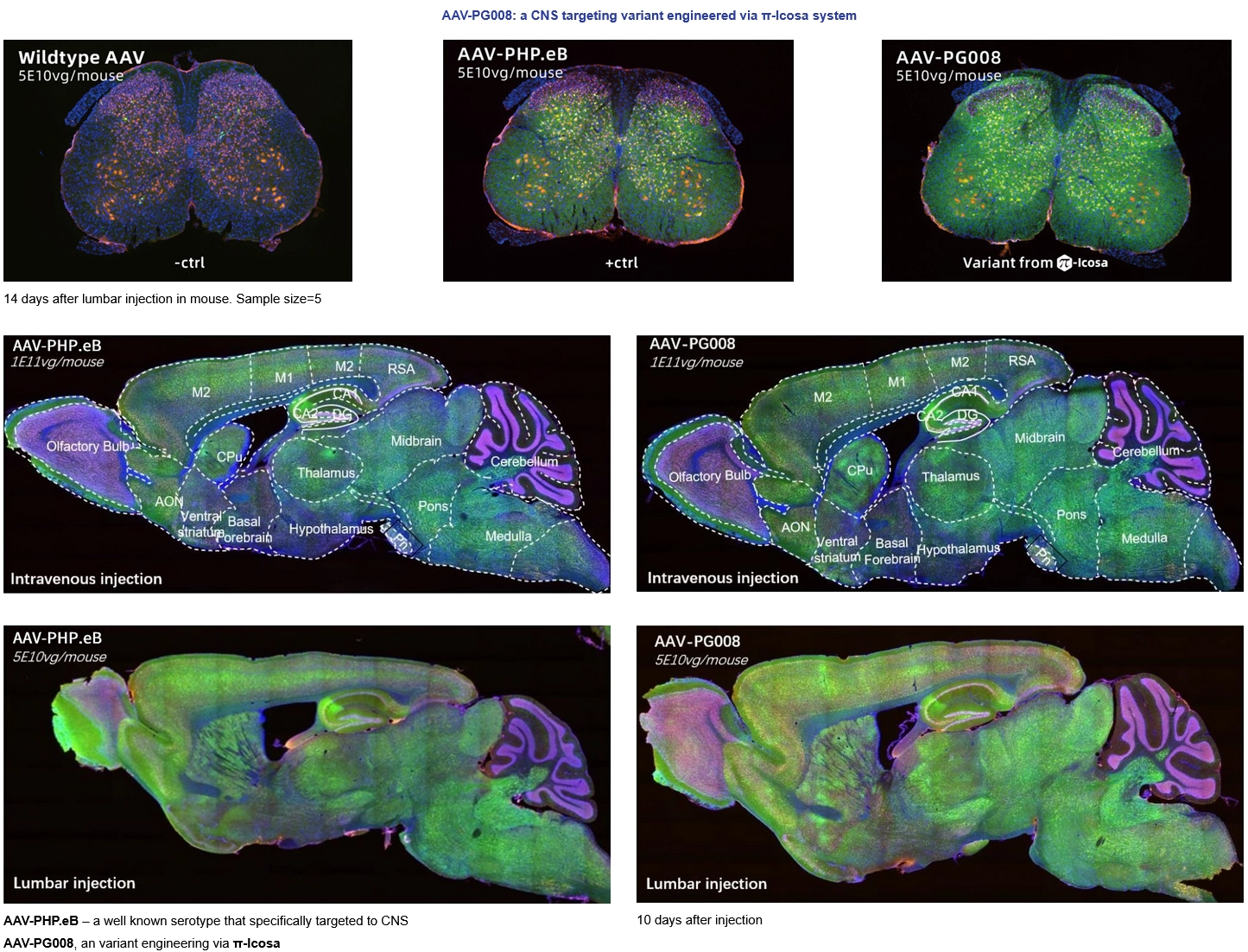
π-lcosa システムからスクリーニングされた新規キャプシドは中枢神経系(CNS)を標的とする
-
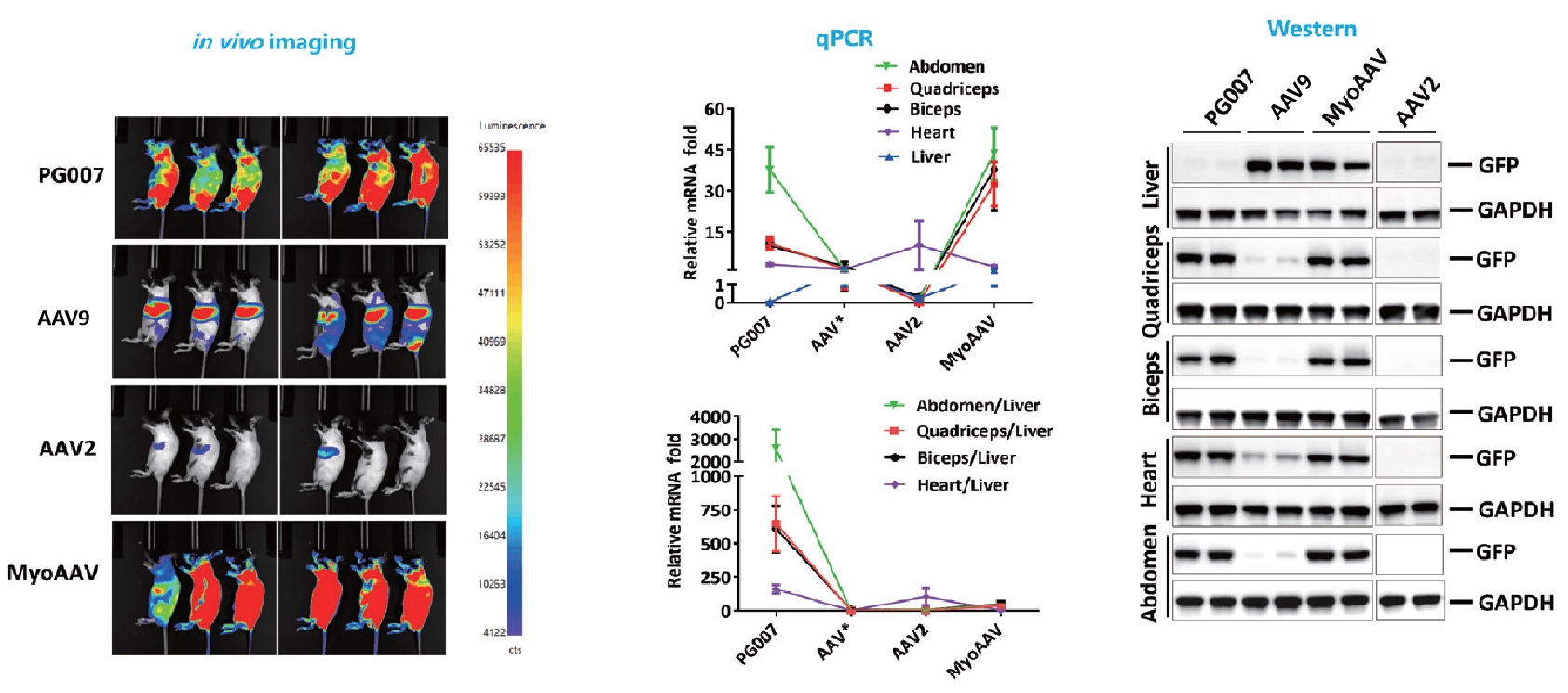
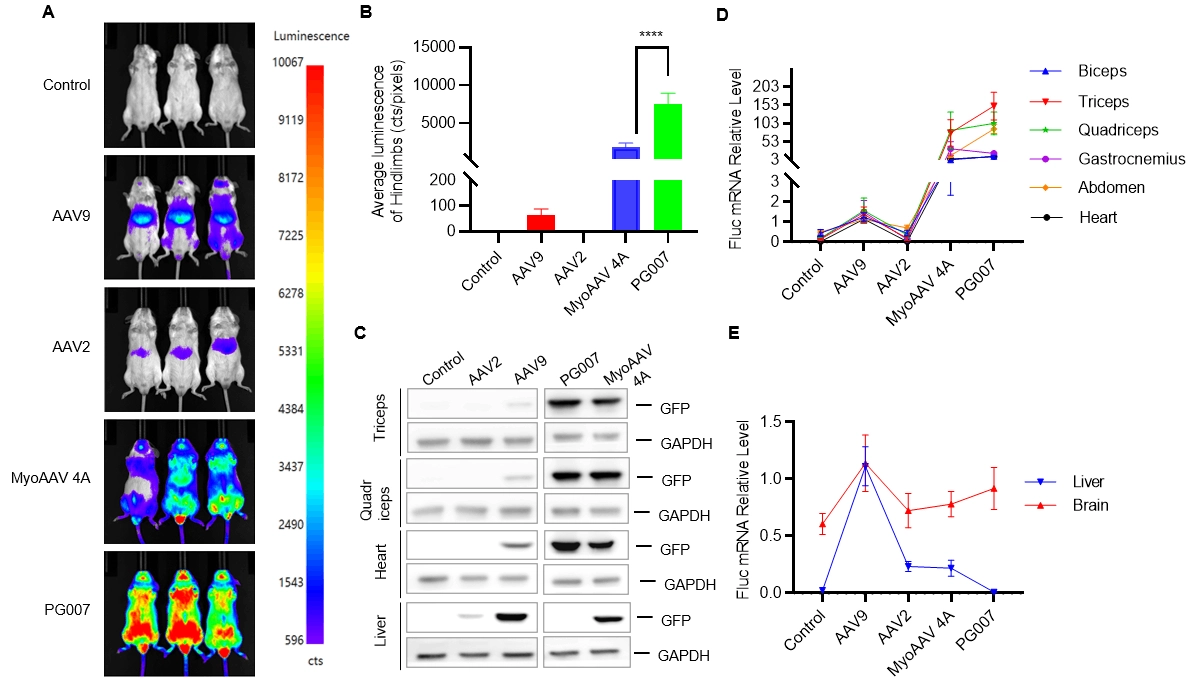
肝臓脱標的化を伴う筋肉標的化新規キャプシド
-
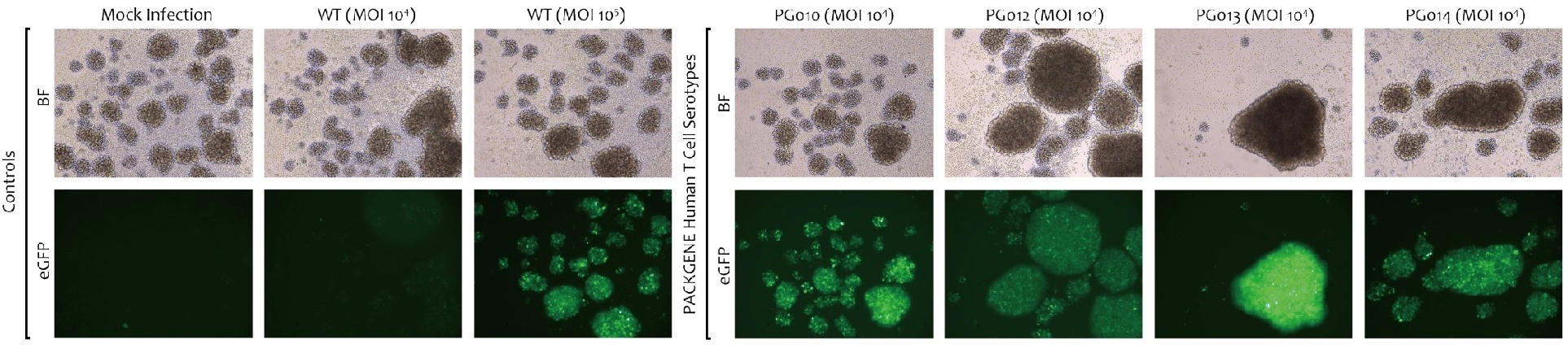
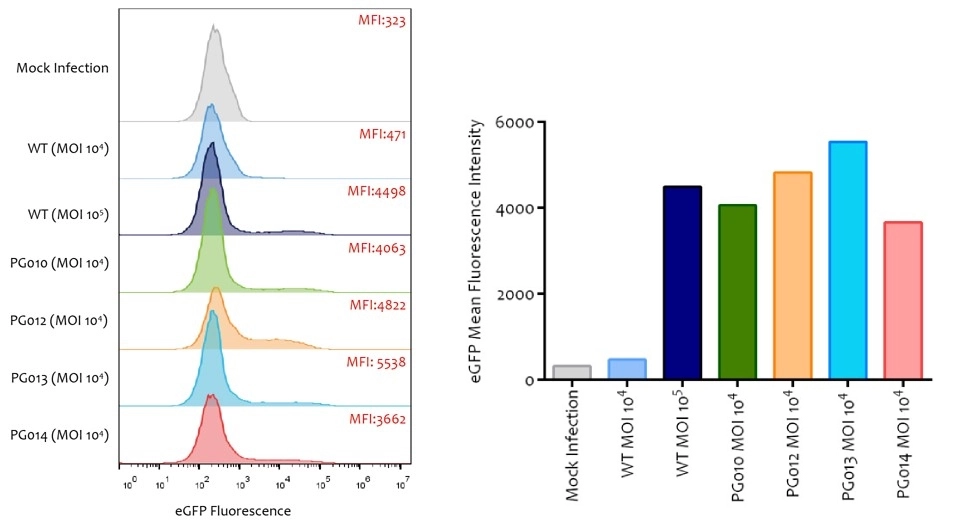
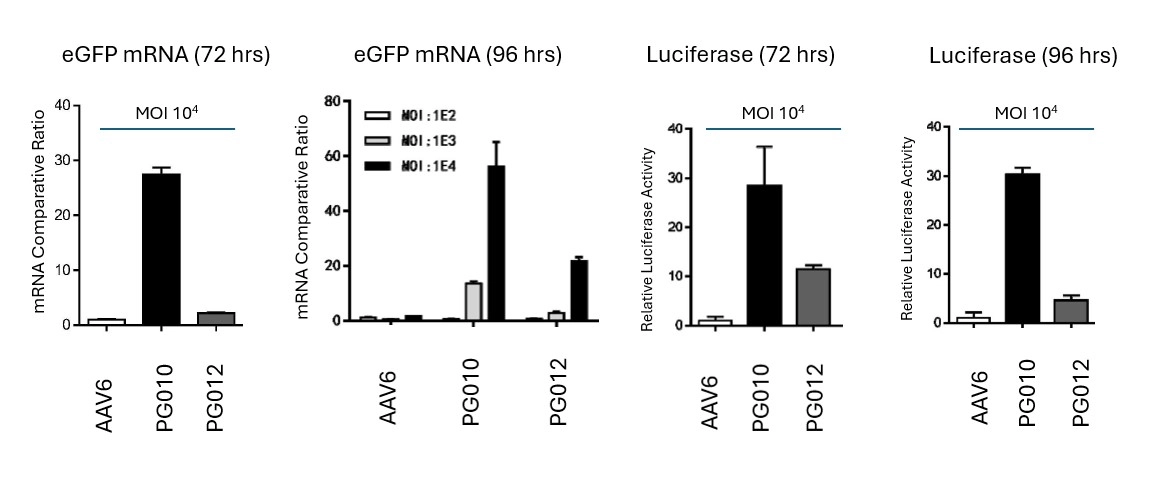
ヒト初代 T 細胞を標的とする新規キャプシド