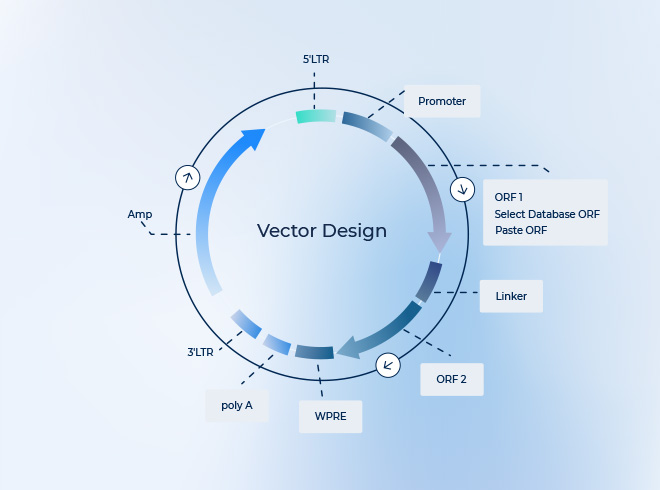
アデノ随伴ウイルス(AAV)のパッケージングは、安定した高滴度ウイルスを得るために非常に繊細なプロセスで、いくつかの一般的な問題がよく見られます。
1. 低ウイルス滴度
原因の例:
-
トランスフェクション効率が低い(プラスミド質量や比率が不適切)
-
細胞の健康状態が悪い(過密、栄養不足、感染など)
-
ウイルスカプシドの遺伝子やパッケージングプラスミドの品質不良
対策:
-
高品質なプラスミドを使用する
-
トランスフェクション条件(試薬量、細胞密度)を最適化
-
健康な細胞で作製
2. 異物混入・細胞破壊による不純物の混入
原因の例:
-
過剰な細胞破砕
-
不十分な精製ステップ
-
培養中の汚染(細菌、真菌)
対策:
-
適切なウイルス回収方法(メディア収集と低速遠心など)
-
精製プロトコールの徹底(イオン交換、CsCl勾配、PEG沈殿など)
-
無菌操作を徹底
3. ウイルスの不活性化
原因の例:
-
高温やpH変化によるカプシドの変性
-
凍結融解の繰り返し
-
強い界面活性剤や金属イオンによる影響
対策:
-
適切な保存条件(-80℃、凍結融解は最小限)
-
保存バッファーの選定(生理的pH、適切な添加剤)
4. 遺伝子挿入サイズが大きすぎる
AAVは一般に最大約4.7 kbまでしかパッケージングできません。
影響:
-
ウイルス粒子の形成効率が低下
-
滴度が低下
-
部分的な断片ウイルスの生成
対策:
-
遺伝子サイズを小さくする(必須エレメントのみ)
-
スプリットAAV戦略を検討
5. カプシド血清型による制限
-
血清型によってパッケージング効率や細胞への感染効率が異なる
-
一部の血清型は特定の細胞で低効率になることがある
対策:
-
標的細胞に適した血清型を選定
-
必要に応じて血清型をスワップしてテスト
6. DNAリコンビネーションや欠損
-
長期間培養されたプラスミドやパッケージング用細胞株でリコンビネーションが起こると、カプシドやI TR 配列が欠損してしまう
対策:
-
新鮮なプラスミドと細胞株を使用
-
過剰培養を避ける
AAVパッケージングの問題の多くは「細胞の健康」「プラスミドの品質」「遺伝子挿入サイズ」「保存・精製条件」に起因します。プロトコールの最適化と各ステップでの品質管理が鍵です。
PackGeneについて
PackGene Biotech is a world-leading CRO and CDMO, excelling in AAV vectors, mRNA, plasmid DNA, and lentiviral vector solutions. Our comprehensive offerings span from vector design and construction to AAV, lentivirus, and mRNA services. With a sharp focus on early-stage drug discovery, preclinical development, and cell and gene therapy trials, we deliver cost-effective, dependable, and scalable production solutions. Leveraging our groundbreaking π-alpha 293 AAV high-yield platform, we amplify AAV production by up to 10-fold, yielding up to 1e+17vg per batch to meet diverse commercial and clinical project needs. Moreover, our tailored mRNA and LNP products and services cater to every stage of drug and vaccine development, from research to GMP production, providing a seamless, end-to-end solution.