AAV(アデノ随伴ウイルス, adeno-associated virus)は、動物実験において極めて広く用いられている遺伝子導入ベクターであり、特に遺伝子送達、遺伝子機能解析、疾患モデルの作製、および遺伝子治療の前臨床研究において重要な役割を果たしている。
1. 動物実験におけるAAVの主な応用
1.1 遺伝子過剰発現
目的遺伝子をAAVベクターに搭載して動物体内へ投与することで、特定組織において安定した発現を誘導することができる。
主な用途:
- 特定遺伝子が疾患発症に関与するかの検証
- 脳、肝臓、心臓、筋肉、網膜などにおける外来性タンパク質の発現
- GFPやmCherryなどの蛍光タンパク質を用いた標識・追跡
1.2 遺伝子ノックダウンまたは発現抑制
AAVは以下のような発現カセットを搭載可能である:
- shRNA
- miRNA発現配列
- 一部の条件下におけるCRISPR関連要素
これにより標的遺伝子の発現を抑制し、その生理学的・病理学的機能を解析することが可能である。
応用例:
- 神経科学分野における受容体やイオンチャネルのノックダウン
- がん研究における癌遺伝子の抑制
- 代謝研究における重要酵素遺伝子のサイレンシング
1.3 疾患モデル動物の作製
AAVを用いて成体動物に疾患関連遺伝子または変異遺伝子を導入し、疾患モデルを迅速に構築することができる。
例:
- パーキンソン病モデル:黒質または線条体における α-synuclein の発現
- アルツハイマー病モデル:APP や Tau 変異体の発現
- 心筋症モデル:心筋における変異タンパク質の過剰発現
- 肝疾患モデル:代謝異常関連遺伝子の導入
この方法は、従来のトランスジェニック動物作製法よりも迅速である。
1.4 神経回路標識およびトレーシング研究
AAVは神経科学研究において特に汎用されている。
主な用途:
- 特定神経細胞群の標識
- 順行性あるいは局所的トレーシング
- Cre-LoxPシステムとの併用による細胞型特異的発現
- カルシウムプローブ(GCaMP)、光遺伝学ツール(ChR2、NpHR)、化学遺伝学ツール(DREADDs)の発現
代表的実験例:
- マウス脳領域に AAV-CaMKII-GFP を注入し、興奮性ニューロンを標識
- Creマウスに AAV-DIO-ChR2 を注入し、特定神経細胞群を光遺伝学的に操作
1.5 遺伝子治療の前臨床研究
AAVは遺伝子治療研究で最も一般的に使用されるベクターの一つであり、動物実験では以下を評価するために用いられる。
- 治療遺伝子が有効に発現するか
- 疾患表現型が改善されるか
- 安全性および毒性
- 最適な投与量および投与経路
主な対象疾患:
- 血友病
- 遺伝性網膜疾患
- 脊髄性筋萎縮症
- デュシェンヌ型筋ジストロフィー
2. 動物実験におけるAAVの主な利点
利点
- 免疫原性が比較的低い
- 安全性が高い(病原性ウイルスではない)
- 分裂細胞および非分裂細胞の双方に感染可能
- 体内で比較的長期間の発現が可能
- 多様な血清型が存在し、組織指向性が異なる
3. 主なAAV血清型とその応用傾向
| 血清型 | 主な特徴/標的組織 |
| AAV2 | 中枢神経系研究で広く使用される古典的血清型 |
| AAV5 | 脳組織、網膜への導入に適する |
| AAV8 | 肝臓への高い導入効率 |
| AAV9 | 心臓、筋肉に高効率、一部では血液脳関門通過能を有する |
| PHP.eB / PHP.S | マウス中枢・末梢神経系で高効率。ただし系統差に注意が必要 |
実際の選択は、動物種、標的組織、投与方法、プロモーター設計に基づいて判断する必要がある。
4. 主な投与方法
4.1 局所投与
- 脳内定位注入
- 筋肉内注射
- 眼内注射
- 関節腔内注射
利点: 高い局在性、比較的少量で効果が得られる
欠点: 高度な手技を要する
4.2 全身投与
- 尾静脈注射
- 腹腔内注射
- 新生児マウスにおける顔面静脈注射
利点: 全身性遺伝子送達に適する
欠点: 高用量を要し、オフターゲットおよび免疫応答の問題が生じやすい
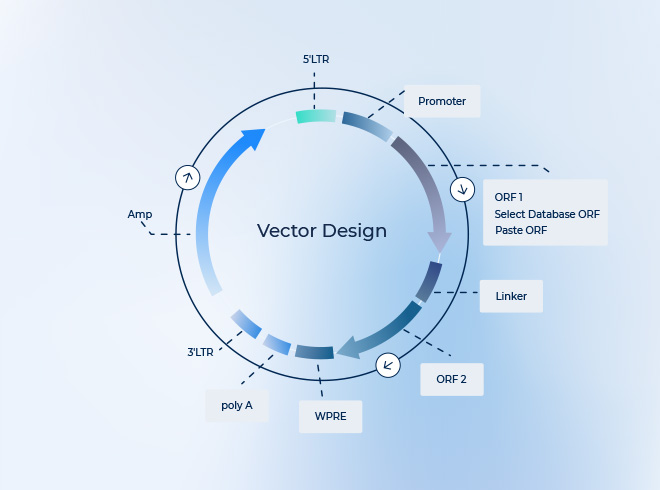
5. AAVベクター設計における主な考慮事項
5.1 プロモーターの選択
どの細胞・組織で発現させるかを規定する重要な要素である。
例:
- CMV:広範囲で強力な発現
- CAG:強力で汎用性が高い
- hSyn:神経細胞特異的
- GFAP:アストロサイト特異的
- CaMKII:興奮性ニューロンに適する
- Albumin / TBG:肝細胞特異的
5.2 パッケージング容量の制限
AAVの最大搭載容量はおよそ 4.7 kb であり、これは重要な制約となる。
遺伝子サイズが大きい場合には、以下の方法を検討する:
- デュアルAAVシステム
- 短縮型遺伝子の使用
- 他のウイルスベクター(レンチウイルス、アデノウイルスなど)の利用
6. AAVの限界
- 搭載容量が小さい
- 一部組織では導入効率が限定的
- 免疫応答を誘導する可能性がある
- 高用量全身投与では肝毒性や炎症反応のリスクがある
- 発現開始までに通常 1~4週間 あるいはそれ以上を要する
- 動物種や系統によって導入効率や発現パターンに差がある
7. 動物実験デザインにおける留意点
実験前に以下を明確にする必要がある:
- 1.研究目的:過剰発現、ノックダウン、トレーシング、治療評価のいずれか
- 2.標的組織:脳、肝臓、心臓、筋肉など
- 3.血清型の選択
- 4.プロモーターの選択
- 5.投与経路
- 6.用量設定
- 7.発現までの時間
- 8.対照群の設定
主な対照群
- 空ベクターAAV群
- AAV-GFP群
- sham注射群
- 野生型または未処置群
8. まとめ
AAVの動物実験における中核的価値は以下の通りである。
- 高効率な遺伝子送達
- 組織・細胞特異的発現の実現
- 長期的研究への適用性
- 神経科学、循環器、肝疾患、筋疾患、および遺伝子治療研究への広範な応用
PackGeneについて
PackGene Biotech is a world-leading CRO and CDMO, excelling in AAV vectors, mRNA, plasmid DNA, and lentiviral vector solutions. Our comprehensive offerings span from vector design and construction to AAV, lentivirus, and mRNA services. With a sharp focus on early-stage drug discovery, preclinical development, and cell and gene therapy trials, we deliver cost-effective, dependable, and scalable production solutions. Leveraging our groundbreaking π-alpha 293 AAV high-yield platform, we amplify AAV production by up to 10-fold, yielding up to 1e+17vg per batch to meet diverse commercial and clinical project needs. Moreover, our tailored mRNA and LNP products and services cater to every stage of drug and vaccine development, from research to GMP production, providing a seamless, end-to-end solution.