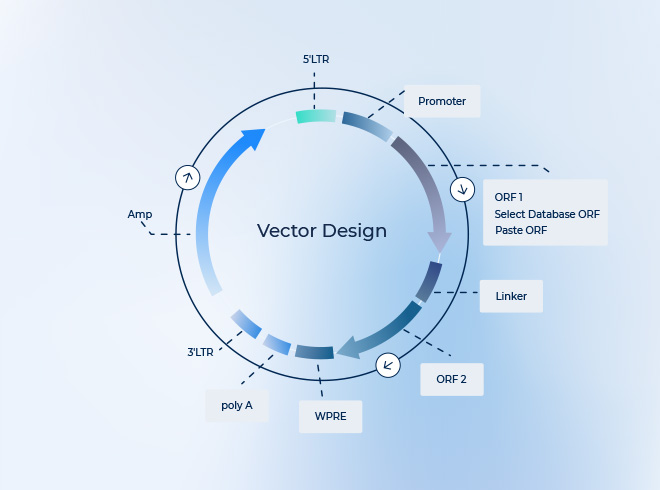
アデノ随伴ウイルス(AAV)を用いた動物実験では、目的遺伝子が十分に発現しない、蛍光シグナルが弱い、個体差が大きい、同じ条件でも再現性が安定しない――このような問題に直面することは少なくありません。
一見すると「発現しない」「シグナルが弱い」という単純な現象に見えても、実際にはベクター設計、ウイルス品質、投与手技、解析タイミングなど、複数の工程が関与しています。AAV実験は一連のプロセスで成り立っており、どこか一つに問題があるだけでも最終結果に大きく影響します。
本稿では、AAV動物実験でよく見られるトラブルの原因と、実践的な改善ポイントを工程ごとに整理して解説します。
1. まず確認すべきは「全く発現しない」のか、「発現はあるが弱い」のか
結果が想定より悪い場合、最初に行うべきことは原因の切り分けです。
全く発現しない場合に考えられる主な要因
- 使用したプロモーターが標的組織に適していない
- ウイルスが目的部位へ到達していない
- ウイルス活性の低下、失活
- ベクター構築ミス
- 観察時期が早すぎる
- 中和抗体などによる感染阻害
発現はあるが弱い場合に多い要因
- ウイルス力価不足
- 血清型(セロタイプ)の選択不適切
- プロモーター活性が弱い
- 蛍光タンパク質の輝度不足
- 撮像条件が最適化されていない
- 挿入配列が長すぎて包装効率が低い
この二つは対策が異なるため、最初の判断が重要です。
2. ベクター設計は実験成功率を左右する重要因子
プロモーター選択の重要性
組織・細胞種によって適したプロモーターは異なります。
- 神経細胞:hSyn、CamKII
- アストロサイト:GFAP
- 肝臓:TBG
- 心筋:cTnT
- 広範発現:CAG、CMV
CMVは汎用的に用いられますが、組織によっては長期的にサイレンシングされる場合があります。特に中枢神経系では注意が必要です。
AAVの搭載容量制限
AAVの搭載可能サイズは一般に約4.7 kbとされます。これを超えると、
- 力価低下
- 不完全包装
- 発現低下
- 個体差増大
などが起こりやすくなります。
不要配列の削減や短縮型プロモーターの使用も有効です。
レポーター遺伝子の選択
蛍光が弱い場合、発現量ではなく蛍光タンパク質の性能が原因であることもあります。
- 緑色系:EGFP
- 赤色系:tdTomato(高輝度)
- 深部観察:赤色~遠赤色系が有利
3. ウイルス品質の確認は必須
力価が高くても高品質とは限らない
qPCRによるVG/mL値が高くても、感染能を持つ粒子数が十分とは限りません。重要なのは「数」だけでなく「機能」です。
空カプシド比率
empty capsid(空粒子)が多いと、
- 細胞受容体を占有する
- 免疫応答を誘導しやすい
- 実際の導入効率が低下する
といった問題が生じます。
保存条件
AAVは保存条件の影響を受けやすく、
- 凍結融解の繰り返し
- 室温放置
- 吸着しやすいチューブ使用
などで性能低下が起こり得ます。
小分け保存し、-80℃で管理することが推奨されます。
4. セロタイプ選択は組織指向性に直結する
代表例として、
- AAV9:心筋、筋肉、全身投与
- AAV8:肝臓
- AAV2:局所脳投与
- 改変型カプシド:中枢神経系
目的組織に適したセロタイプを選ばなければ、十分な発現は期待できません。
5. 投与手技による影響は大きい
脳定位注入で多い問題
- 座標ずれ
- 注入速度過多による逆流
- 針先閉塞
- 抜針が早すぎる
尾静脈投与で多い問題
- 血管外漏出
- 皮下注入
- 急速投与
技術的要因だけで結果が大きく変わるため、操作の標準化が重要です。
6. 評価時期が早すぎるケースは多い
AAVは導入後すぐには十分発現しません。
- 3日:弱い
- 1週間:発現開始
- 2週間:明瞭
- 3~4週間:ピーク
脳組織では3週間以降に評価する方が安定した結果を得やすい傾向があります。
7. 蛍光観察条件も見直すべきポイント
発現していても、
- 過固定による退色
- 厚切片による透過低下
- レーザー出力不足
- Gain設定不適切
- フィルター不一致
などで弱く見えることがあります。
8. トラブル時の推奨確認フロー
- プラスミド構築確認
- ウイルス活性確認
- 投与成功確認
- 観察時期再検討
- セロタイプ・プロモーター・投与量見直し
9. まとめ
AAV動物実験は、単なるウイルス投与実験ではなく、設計・製造・投与・解析まで一体となった総合技術です。結果が不十分な場合も、原因を段階的に整理すれば改善できるケースは少なくありません。
細部を標準化し、論理的にトラブルシュートすることが、成功率向上への近道です。
PackGeneについて
PackGene Biotech is a world-leading CRO and CDMO, excelling in AAV vectors, mRNA, plasmid DNA, and lentiviral vector solutions. Our comprehensive offerings span from vector design and construction to AAV, lentivirus, and mRNA services. With a sharp focus on early-stage drug discovery, preclinical development, and cell and gene therapy trials, we deliver cost-effective, dependable, and scalable production solutions. Leveraging our groundbreaking π-alpha 293 AAV high-yield platform, we amplify AAV production by up to 10-fold, yielding up to 1e+17vg per batch to meet diverse commercial and clinical project needs. Moreover, our tailored mRNA and LNP products and services cater to every stage of drug and vaccine development, from research to GMP production, providing a seamless, end-to-end solution.