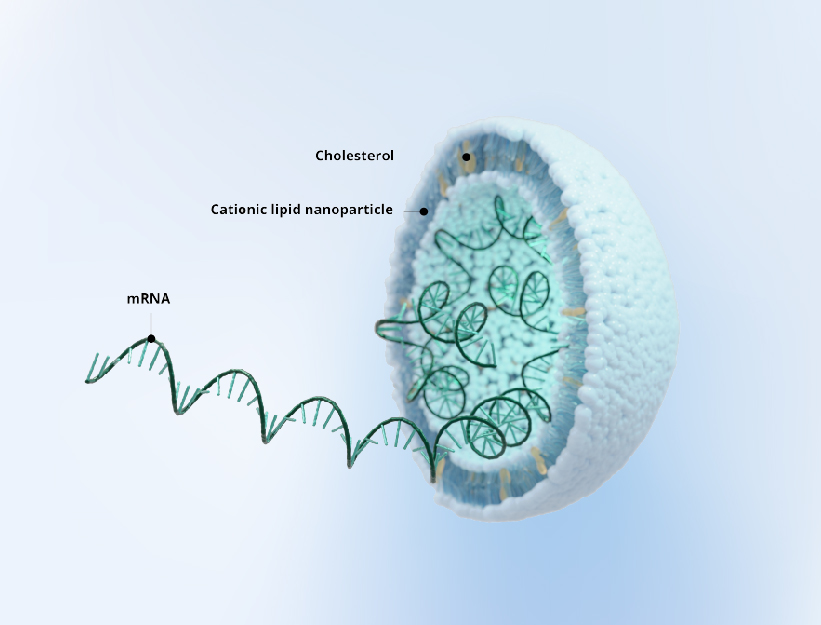
mRNA技術は、ワクチン、がん治療、遺伝子編集などの分野で急速に発展しており、mRNA-LNP(脂質ナノ粒子)は現在もっとも重要な送達プラットフォームの一つとされています。研究室レベルでは mRNA-LNP の調製が可能でも、臨床開発や商業生産へ進むためには、GMP(Good Manufacturing Practice:医薬品の製造管理および品質管理基準)に適合した製造体制が必要です。
これは単に「製造できる」ということではなく、品質の安定性、ロット間の一貫性、工程のトレーサビリティ、そして規制要件への適合が求められることを意味します。では、GMPグレード mRNA-LNP 製造では、どのような点に注意すべきなのでしょうか。
1. 原材料の品質管理が出発点
GMP製造において、最初に重視されるのは原材料の品質です。mRNA-LNP では、大きく分けて mRNA原液 と 脂質原料 の2つがあります。
mRNA原液
mRNA自体の品質は最終製剤の性能に直結するため、以下の項目を確認する必要があります。
- 配列の正確性
- キャップ構造(Cap)の完全性
- Poly(A) tail 長の均一性
- 二本鎖RNA(dsRNA)不純物の残留
- 分解体・短鎖RNAの有無
- エンドトキシン
- RNase汚染
特に dsRNA は、意図しない自然免疫応答を誘導する可能性があり、重要な管理項目です。
脂質原料
LNPは一般的に以下の4成分で構成されます。
- イオン化脂質(Ionizable lipid)
- DSPC
- コレステロール
- PEG脂質
これらの純度、安定性、ロット間再現性は極めて重要です。特にイオン化脂質の品質変動は、粒径、封入率、体内送達効率に大きく影響します。
2. 製造条件が製剤特性を左右する
mRNA-LNP は通常、エタノールに溶解した脂質相と、mRNAを含む水相を高速混合し、自己組織化によって形成されます。
シンプルな工程に見えても、実際には工程条件の最適化が非常に重要です。
主な管理パラメータ
流量比(FRR)
水相と有機相の体積比であり、粒径や封入率に影響します。
総流量(TFR)
混合速度に関与し、粒子径分布や均一性に影響します。
pH条件
一般に酸性条件下で脂質を陽電荷化し、mRNAとの複合化を促進します。pHが不適切だと封入率低下やRNA損傷につながります。
N/P比
陽イオン性脂質とRNAリン酸基との比率であり、送達効率と安全性の重要指標です。
3. スケールアップは単純な増量ではない
研究段階では良好な結果が得られても、GMPスケールへ移行した際に品質特性が変化するケースは少なくありません。
LNP形成は瞬間的な混合環境に大きく依存するため、装置構造、流路設計、剪断力、流速条件の違いが製剤品質に直結します。
そのため、スケールアップ時には単なる容量拡大ではなく、技術移管(Tech Transfer)および同等性評価(Comparability Study)が不可欠です。
4. 無菌管理とRNase対策
mRNA-LNP は注射製剤として使用されることが多く、無菌製造管理が必須です。
さらに mRNA製剤特有のリスクとして RNase汚染 があります。RNase は環境中や人体由来で広く存在し、わずかな混入でもRNAを分解する可能性があります。
そのため、以下の対応が求められます。
- RNase-free資材の使用
- 専用洗浄手順
- 作業員教育
- 環境モニタリング
5. 品質試験体制の整備
GMP製品では、出荷判定のために包括的な試験体制が必要です。
主な試験項目
物理化学特性
- 粒径
- PDI(多分散指数)
- ゼータ電位
- pH
- 浸透圧
RNA関連
- RNA濃度
- 完全性
- 封入率
- dsRNA残留
- DNAテンプレート残留
安全性
- 無菌試験
- エンドトキシン
- 残留溶媒(エタノール等)
生物活性
- 細胞発現試験
- Potency assay(力価試験)
6. 安定性評価が実用化の鍵
mRNA-LNP は比較的不安定であり、以下の影響を受けやすい特徴があります。
- 温度変動
- 凍結融解
- 酸化
- 凝集
- RNA加水分解
このため、糖類(スクロース、トレハロース等)を添加し、低温保存されることが一般的です。
さらに、
- 長期安定性
- 加速安定性
- 使用時安定性
- 輸送時安定性
などの評価が必要です。
7. GMPは製造だけでなく管理体制でもある
GMPは単なる製造基準ではなく、品質保証システム全体を指します。
各ロットについて、以下の記録が必要です。
- 原材料情報
- 製造記録
- 設備状態
- 作業記録
- 逸脱・変更管理
- 試験結果
これらは規制当局査察時にも重要な確認対象となります。
8. まとめ
GMPグレード mRNA-LNP 製造は、研究室レベルの製剤化を工業生産へ移行するだけの作業ではありません。原材料管理、工程設計、スケールアップ、品質評価、安定性試験、品質保証体制まで含めた総合的な取り組みが必要です。
PackGeneについて
PackGene Biotech is a world-leading CRO and CDMO, excelling in AAV vectors, mRNA, plasmid DNA, and lentiviral vector solutions. Our comprehensive offerings span from vector design and construction to AAV, lentivirus, and mRNA services. With a sharp focus on early-stage drug discovery, preclinical development, and cell and gene therapy trials, we deliver cost-effective, dependable, and scalable production solutions. Leveraging our groundbreaking π-alpha 293 AAV high-yield platform, we amplify AAV production by up to 10-fold, yielding up to 1e+17vg per batch to meet diverse commercial and clinical project needs. Moreover, our tailored mRNA and LNP products and services cater to every stage of drug and vaccine development, from research to GMP production, providing a seamless, end-to-end solution.